Quelle volume de carburant produit une seule fourmi?
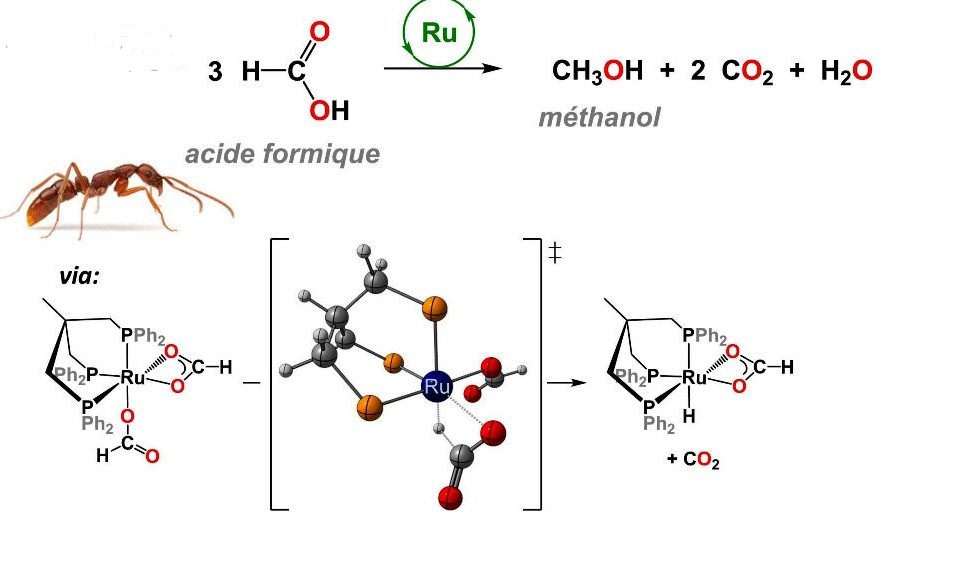
On sait qu’une fourmi expulse en moyenne 3×10^-3 ml (10^-3 veut dire 10 puissance -3) d’acide méthanoïque (ou acide formique) de masse volumique égal à 1.22 g/cm3 (données internet). Il faut donc calculer la quantité de matière de cette valeur pour pouvoir ensuite appliquer le catalyseur car le rendement chimique se fait avec des valeurs en mol.
Donc masse de l’acide formique = masse volumique x volume
= 1.22 x 3×10^-3
= 3.66×10^-3 g.
La masse d’acide formique expulsée par une fourmi est donc égal à 3.66×10^-3 gramme.
Pour calculer ensuite la masse molaire de celle-ci nous avons besoin de sa composition exposée dans la formule ci-dessus.
Sachant d’après le tableau périodique que H=1 g/mol, que O=16 g/mol, et que C=12 g/mol.
La masse molaire de l’acide formique est donc égal à la somme de ces valeurs:16+1+12+16+1=46 g/mol.
La masse molaire de l’acide formique est donc égal a 46 g/mol.
Nous pouvons donc maintenant calculer la quantité de matière de l’acide formique expulsé par une fourmi grâce à la formule suivante:
quantité de matière= masse/masse molaire
Donc: (3.66×10^-3)/46= 7.95×10^-5 mol.
La quantité de matière d’acide formique expulsée par une fourmi est donc égal à 7.95×10^-5 mol.
Ensuite s’applique le Catalyseur de ruthénium avec un rendement de 50% donc: (7.95×10^-5)/2= 3.97×10^-5 mol transformée en méthanol.
Après la réaction chimique on obtient donc 3.97×10^-5 mol de méthanol.
On utilise ensuite la formule ci dessus pour calculer la masse molaire du méthanol sachant que H=1 g/mol, O=16 g/mol, et que C=12 g/mol.
Donc masse molaire=1+1+1+1+12+16=32 g/mol.
La masse molaire du méthanol est donc égale à 32 g/mol.
Pour obtenir la masse de ce méthanol obtenue on utilise donc la formule suivante: masse=quantite de matiere x masse molaire.
Donc (3.97×10^-5)x32= 1.27×10^-3 g.
La masse de ce méthanol est donc égale à 1.27×10^-3 gramme.
Nous savons ensuite (d’après Wikipédia) que la Masse volumique du méthanol est égale à 0.7910 g/cm3.
Donc pour calculer le volume de méthanol obtenue on utilise la formule suivante: volume= masse / masse volumique.
Ce qui est donc égal à: (1.27×10^-3)/0.7910=1.60×10^-3 cm3.
Donc est égal à 1.60×10^-3 ml soit 0.0016 ml et 0.0000016 L.
Donc une fourmi produit 0.0016 ml de méthanol.
Donc pour produire un litre: 1/0.0000016= 625 000.
Il faudrait donc 625 000 fourmis pour produire un litre de méthanol.
A ce stade on peut se dire que ce n’est pas très rentable cependant si l’on prend la population mondiale de fourmis formica et le temps qu’une fourmi met à produire son acide formique cela pourrait complétement changer la donne. Malheureusement malgré de nombreuses recherches ainsi que des inscriptions dans des forums de myrmécologie (science liée à l’entomologie spécialisée dans l’étude des fourmis) nous n’avons trouvé aucune réponse car ces chiffres peuvent énormément varier en fonction de L’espèce du temps etc…
Mais prenons l’exemple d’une des plus grosses fourmilière de formica polyctena (plus précisément des formica lugubris) située dans le parc jurassien vaudois en suisse, cette fourmilière compte à elle seule 200 millions d’individus.
200 000 000/625 000=320
Cette fourmilière à elle seule produirait donc 320 litres de méthanol par jour soit 116 800 par an ce qui n’est pas énorme mais non négligeable non plus. Et de plus il faudrait qu’une fourmi puisse produire son acide formique en une journée mais comme cette information est totalement fictive il est très difficile pour l’instant de déterminer si cela est réellement rentable.

